����ҩΪ��ƵƵ�����飿 | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| http://www.sina.com.cn 2006��08��30��09:10 ��Ͽ��-�����ձ� | |||||||||||||
|
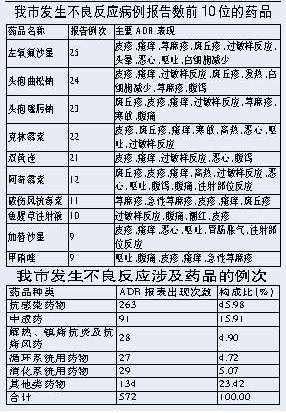
������ҩ�����ر�����ʾ�������ϰ�����256��ҩƷ���ֲ�����Ӧ���漰����Ϊ����Ⱦҩ�� ��������Ե�� ����Ϊ��ǿҩƷ������Ӧ��⡢���湤�����ƽ�������ҩ�����Ϲ�����ҩ��ȫ��Ч����
�������˽⣬�ӽ����ϰ����ϱ���412�ݱ��漶���������µ����ص�ADR����Ϊ2�����µ�һ���12�������ص�19����һ���385���������µġ����ص�ռ8.01%�� ����
������Ϊ�л��߳��ֲ�����Ӧ������������������Ϊ�������� ������ס˼��������·����ҽ������������ǰ����߷�ӳ���������ӳ�ΪҩƷ������Ӧ���ܺ��ߣ�������������ή����ÿ��Ҫ����4�Σ�һ���ҽҩ�Ѿ�Ҫ8���Ԫ����ҽ���Ļ��ü�����һ����˵��ҽ������ҩ֪ʶ��Էḻ���������ǵ����˶�û�ӹ�ҩƷ������Ӧ���˺�������˵������Щ��ҩ֪ʶ�ġ����⺺���ˡ� ������ҩ��ֽ��ն�2006���ϰ��������ϱ���412��ҩƷ������Ӧ��ADR����������˷�����ҩ����Ա˵�����ϱ���412�ݱ��漶��������68.93%��Ҫ������7���м�ҽ�ƻ���������ȥ��ͬ�ڱ��浥λ����14������������289������нϴ���ߣ���ҩƷ��������Ӫ��ҵ����һ���ϱ�������ȫ�еı���������ƫ�٣��µġ����صIJ�����Ӧ������ƫ�ͣ���ռ8%������˵���������ADR�ϱ�������Ȼ��һ���Ͼ��Ŀ��⡣�������ն�ҩ��ַ���������ص���н���� �������ݡ�ҩƷ������Ӧ����ͼ������취����ҩƷ������Ӧ��ADR����ָ�ϸ�ҩƷ�������÷������£����ֵ�����ҩĿ���صĻ�����֮����к���Ӧ�����������������ⳬ������ҩ����ķ�Ӧ�Լ���ҩ��������ķ�Ӧ�� �����ص���� ����1.������ ���� �������飺�ٴ���Ӧ�ü�ǿ����Ⱦҩ��ĺ���ʹ�� ������572���ε�ADR���������У��漰����ҩ��Ϊ����Ⱦҩ�ҩ����Ա����˵�����뿹��Ⱦҩ�����ٴ��㷺Ӧ�������й�ϵ����������ʾ���ŵͪ�ࡢͷ�߾����ࡢ��ù����ʹ��������ٴ�ADR�����ʽϸߡ� ������ͳ�ƣ���263���ο���Ⱦҩ�ﲻ����Ӧ�����У���������ҩ�������ߣ�ռ����Ⱦҩ��������60.29%����������ͷ�߾����ࣨ83���Σ����ŵͪ�ࣨ61���Σ�����ù���ࣨ27���Σ����ֿ�ù���ࣨ25���Σ����������ࣨ21���Σ�������ҩ��λ��ADR����������ǰ5λ�������ٴ���ʹ���ʽϸ��йء� �����й�ר��ָ��������Ⱦҩ��Ĵ���ʹ�ã�����������ϸ����ҩ���꣬����ʹ�������ھ�Ⱥʧ��������ʹ��Ч���ͣ����˵IJ�����Ӧ���࣬ͬʱ��ɿ���Ⱦҩ��Ŀ�����ҩ����ˣ��ٴ���Ӧ�ü�ǿ����Ⱦҩ��ĺ���ʹ�ã����ٻ������ҩ���������Ƴ̹����Ȳ���������ķ����� ����2.������ע ���� �������飺��ǿ������Һ������� ������רҵ��ʿ���ܣ���ҩ;����ͬ��ADR�ķ������ͬ�����ϰ����ϱ���412��ADR���������У���ҩ;����Ҫ�о�����ע���ڷ���ҩ������ע�䡢������ҩ��������ҩ��Ƥ��ע�䡢�ֲ���ҩ������ע�䡢ֱ����ҩ��������ҩ�������ҩ�ȡ����������ʾ��������ע�Ϳڷ���ҩ�����ϸߣ��ֱ�ռ54.20%��33.39%�� ������ͳ�ƣ�412�ݱ����У�������ע��ҩ��ʽ310���Σ�ռ54.20%��������Щ�������ͳ�ƣ�����ǰʮλ��ҩƷ�У��Ծ�����ҩ��ʽ����8��Ʒ�֣���Ȼ��������ҩ��ADR��������ߡ� �����Դˣ�ҩ����Ա��ʾ�����ǿ������Һ�����������ʹ�ÿڷ�����ע���ܴﵽ����Ŀ�ģ���������ʹ�þ�����ҩ�� �����ر��ע ����1.��ҩ�Ƽ� ���� �������飺��ҩӦ�ϸ�����Ӧ֢��Χʹ�� ����������ҩ��Ӧ�÷�ΧԽ��Խ�㣬��ҩע�����������࣬��ҩ��������ADRҲ�ڲ������ࡣ�ڴ˴��ϱ����г�ҩADR�����У����漰ҩƷ48�֣�91���Ρ���ҩ;����ע���Ϊ��������53���Ρ����У�˫����ע�����ADR���������ҩƷ�оӵ�5λ�� ������ҩ��ADR�ٴ����ֶ�ΪƤ����ġ����ơ����ȡ�������ͷ�Ρ��ļµȣ�ͣҩһ��ʱ���֢״��ʧ�� ����ҩ����Ա˵���ӱ��淴ӳ��������Կ�������ҩ��ADR�漰��Ϲ㣬Ҳ����˵���Ƕ���ҩ����ʶ������ͣ������ҩ������Ȼ���������á�������Ӧ�IJ����ϣ�Ӧ�ϸ�����Ӧ֢��Χʹ�ã�����ҩ�����ʷ��������ʵĻ��ߡ����������ߡ��ķ����ؼ�������Ӧ����ʹ�á� ����2.�ϲ���ҩ ���� �������飺�������ⲻ��Ҫ�ĺϲ���ҩ������ҩע������ʹ�ø�Ӧ���� �������ϱ���412�ݲ��������У��ϲ���ҩ����107����ռ25.97%�����У�����ϲ�1��ҩ�����ϲ�5��ҩ�ҩ����Ա�����ߣ������ϱ������ϲ���ҩ�����벻����Ӧ�����ʳ��������ȡ���ҩƷ��Խ�࣬Խ������ADR����ˣ��ٴ�ҽ������ҩʱ��Ҫע��ѯ�ʻ����Ƿ���ͬʱ��������ҩ�����������������ⲻ��Ҫ�ĺϲ���ҩ������������ҩע������ʹ�ø�Ӧ�������������ܴﵽ������Ч��Ŀ�ģ�����������ADR�ķ����� ����δ���ص� ����1.���껼�� ����412�ݱ����У�������С��Ϊ������һ��������������Ϊ89�ꡣ�������ͳ�ƣ�18������ռ16.26%��18�꣭29��ռ25.24%��30�꣭39��ռ22.33%��40�꣭49��ռ10.19%��50�꣭59��ռ10.92%��60������ռ15.05%�� ����ҩ����Ա������������ֲ�����ADR�ɷ������κ���������Ⱥ�������ڲ�ͬ����λ��ߵ�Ѫ��������ҩ��������ҩ���л�ٶȼ�����й�ٶȲ�ͬ�����Է���ADR�ĸ��ʡ����س̶ȼ������������ͬ�����껼�ߵ��������ܼ��ˡ����Լ������࣬��δ�����������幹�ɼ������������ܵȷ��涼���ܳ��죬������Ӧ�����ļ�����Խϸߡ���412�ݱ����У�С��18��ĺʹ���60����˾���129����ռ31.31%����ҩ����йظ����˱�ʾ����չ�����껼�ߵ�ADR��������Ϊ����ص㡣 ����2.���Ρ�DZ���Լ����Ե�ҩƷ������Ӧ ����������ʾ��Ƥ�����丽����ȫ��������θϵͳ�����и�������ϵͳ�����༰������ϵͳ��ǰ5λ������Ƥ�����丽����ռ36.31%��ռ��λ��Ƥ������Ƥ��Ϊ��������DZ�̬��Ӧ���ֳƳ�����Ӧ��ָ�쳣�ġ��к��ġ������Ե����߷�Ӧ�������ȡ�������ͷʹ��ȫ��������θϵͳ����������ΪŻ�¡���ʹ����к��ռ10.02%�� ����ҩ����Ա��ʾ��Ŀǰ���ٴ����ڹ۲�IJ�����Ӧ����Ƥ����θ����Ӧ�����ȵȣ����˶�ʱ���ڷ�Ӧ��Ϊ����ǿ�ң������ϱ������϶࣬����Щ���۲쵽�ķ�Ӧ�����Ρ�DZ���Լ����Ե�ҩƷ������Ӧ©���ʽϸߡ���һ����ҩ�ಿ�Ž������Ӵ������ȣ��ٽ�ҩƷ������Ӧ������ȫ�桢����ؿ�չ�� ������������ ���� ͨѶԱ ������ ����������� ��������δ�������ֱ���ע��Һ ��������Ѷ ������ ���ࣩ����ʳƷҩƷ�ල��������ǰ����������ͣ���ۺ�ʹ�ü���ŵ����ҩ����˾�����ġ��˲ζ���ע��Һ����������ͪ��A������ע��Һ��������ҩƷ���������մ���ҩ��ֻ�Ϥ�����������̲飬���и���ҩƷ������ҵ��ҽ�ƻ�����δ�������ۻ�ʹ����Щ����ҩƷ�� �������˽⣬����ŵ����ҩ����˾�����ġ��˲ζ���ע��Һ����������ͪ��A������ע��Һ�������ڷ�ע��Һ��������ɿ�����ע��Һ���ͼ��ְ���Ī����ҩ����˾�����ġ�������ע��Һ����Υ���˹���ʳƷҩƷ�ල�����ֹ���ҩƷ˵����������йع涨��������ͣ������������ҵ�ջ��г�����ͨ������ҩƷ��ͬ����ͨ���Ļ��й㶫�����ÿƼ���ҩ����˾�����ġ������ע��Һ���� ����������δ�ӵ��ϼ�ҩ�ಿ�ŵ���ʽ֪ͨ������ҩ������ڽ��ն�����6��ҩƷ�����˳�����飬��Ҫ������ҩƷ��Ӫ��ʹ�õ�λ����ֹͣ���ۺ�ʹ������6��ҩƷ��ͬʱ��������Ҫ�������ʹ����6��ҩƷ�� ������Թ���ʳƷҩƷ�ල�����ֽ��շ����ġ�֪ͨ�������߽���Ҳѯ�������ڶ��ҽԺ���õ��Ĵ���ҩ�����û���⼸��ҩƷ����ҩ��ֵ��й�ר��Ҳ����˵������л�������ʹ�ù���Щҩ�����һ�����ַ��ȵȲ���֢״Ӧ���쵽ҽԺ��� ����������� ��������ҽ����е����ϳ��� ���� ������������Ҫ����������� ��������Ѷ ��ͨѶԱ �Ӻ��� ���� ��С�ࣩ���ڵ�ҽ����е��η��ֲ��ϸ��������̽�����������������գ����ż�����߾ֶ�����˽���ҽ����е��ȫ���ͨ�����ߣ�5675651��5675642���Է������ҽ����е���ʹ�õ�λ��ʱ��þ�ͨ����ȫʹ������� �������˽⣬�þ��ڼ������з��ֽ���ҽ����е��������϶࣬�����ľ�ʾ��־�������IJ����ֲᡢ��Դ��ͷ�������ҹ�����Ҫ��δ����3C��־�ȣ����գ����ݹ����ʼ��ֵܾIJ������ż�����߾ֶ�Ͻ���ڹ�ȥ������ڵļ�����ϲ�ɨ���豸��CT�����˴Ź����豸��MR�������˵��飬ͬʱ������Ϣ�����ƶȣ�Ҫ�����ҽ����е�ۺ�����š����û����Ž�������ҽ����е��������ʱ����������������Ʒ������Ϣ��Ϊ�˹�����ȫ���ͨ�����ߡ� �������ż�����߾�ǿ�����Խ���ҽ����е���뾳���飬һ�����ִ���������ȫ������һ�ɲ���ʹ�ã��͵����ģ�ͬʱ����α����ְ�ȫʹ������Ľ���ҽ����е�������̽������������������ᷢ������Ԥ���� ����
|
| ������ҳ > �������� > �������� > ���� |
| |||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||