风险增加源于报告责任缺失 | ||
|---|---|---|
| http://www.sina.com.cn 2006年06月08日02:50 北京晨报 | ||
|
近日,国家药监局发布《关于暂停使用和审批鱼腥草注射液等7个注射剂的通知》。根据国家药品不良反应监测中心的监测,鱼腥草注射液等7个注射剂在临床应用中出现了多种严重不良反应,甚至有引起死亡病例报告。现有监测和处理药品安全事件机制能否保障公众的健康安全?“7注射剂叫停事件”,再一次引发公众对用药安全的关注。 药品不良反应指合格药品在正常用法用量下出现的与用药目的无关的有害反应,包 括副作用、毒性反应、过敏反应、后遗效应、首剂效应等等。一种药品从研究开发、动物实验、临床试验到审批上市等全部程序,各国规范都十分严谨,然而由于受当时科技认知等客观条件的限制,仍然无法完全避免药物不良反应的发生。有些罕见、迟发、发生于特殊人群的不良反应只有在药品大面积长期使用后才能被发现。例如发现四环素影响骨骼生长已用了10年,认识非那西丁造成肾损害是在75年之后。从某种意义上说,这种“不良”是一种合理存在,是医学进步的必然代价。药品生产企业在药品说明书中必须注明可能产生的不良反应,履行告知责任。发生不良反应事件时,生产企业有责任向药品监管部门报告。这有利于药品监管部门及时对上市后的药品进行再评价,从而保障人民群众的用药安全有效。在国外,如果有资料证明企业知晓药品有某种不良反应而没有在说明书中提示的,患者服用后发生严重不良反应,企业要依法承担高额赔偿。而在我国,由于相关制度缺失,医生常常对药物不良反应避之唯恐不及。这也是我国药品不良反应病例报告少的主要原因之一。 在赔偿方面,国家明文规定用药后出现的不良反应是医院、药厂的一个免责事由,即医院、药厂对药品不良反应的后果不承担任何责任。目前实践中,常采用《民法通则》之公平原则,即由药厂、医院、患者共同分担损失的做法,尽管是不得已的做法,但绝非合理的做法。只有尽快建立药品不良反应补偿救济机制,如参考一些发达国家的做法,让药品生产企业按年销售额的一定比例提取药品不良反应基金,用于受害者的救济、不良反应监测,降低药品不良反应各方无过错当事人的经济损失和风险,才能实现诚信受益,保护企业参与药品不良反应监控的热情。 石晓英
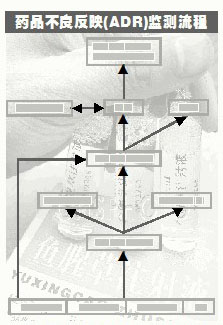
在药害监测流程中,我们在起始阶段,即主体报告阶段就存在很大问题。 ●陈新颖/制图 | ||
| 新浪首页 > 新闻中心 > 综合 > 正文 |
| |||||||||||||
| |||||||||||||||||||||||||||||||||||||||
|
新闻中心意见反馈留言板 电话:010-82612286 欢迎批评指正 新浪简介 | About Sina | 广告服务 | 招聘信息 | 网站律师 | SINA English | 产品答疑 Copyright © 1996-2006 SINA Corporation, All Rights Reserved 新浪公司 版权所有 |