炎琥宁注射剂须黑框警告“接受本品治疗的患者有发生严重过敏反应的风险,包括过敏性休克,严重者可导致死亡。6岁及以下儿童禁用本品”。
国家药监局近日发布公告,要求所有炎琥宁注射剂的上市许可持有人修订说明书,新增黑框警告,明确标注“严重过敏反应可致死亡”,并禁止6岁及以下儿童使用。
此次修订是近年来对中药注射剂最严厉的监管措施之一。黑框警告强调,该药可能引发过敏性休克、呼吸困难等严重反应,且需在具备抢救条件的医疗机构使用。
炎琥宁注射剂用于病毒性肺炎和病毒性上呼吸道感染,是中药注射剂领域的大品种之一。2024年底,炎琥宁注射剂被纳入第三批全国中成药采购联盟集采。作为此次集采竞争最为激烈的品种之一,炎琥宁注射剂产品平均降价86%。公开信息显示,珍宝岛(603567.SH)、一品红(300723.SZ)中标。哈三联(002900.SZ)、复星医药(600196.SH)、莱美药业(300006.SZ)等公司也有炎琥宁注射剂产品在售。
近年来,中药注射剂的安全性和疗效争议不断,而监管层也在不断加强规范中药注射剂的使用。机构数据显示,中药注射剂市场规模近十年来市场缩水近50%。二级市场上,今年以来已经有两家中药注射剂领域的公司走向退市边缘,*ST大药(603963.SH)在近日被终止上市,*ST龙津(002750.SZ)市值仅剩6.1亿元。
多家上市公司涉及其中
根据国家药监局的《关于修订炎琥宁注射剂说明书的公告》,炎琥宁注射剂包括注射用炎琥宁、炎琥宁注射液、炎琥宁氯化钠注射液。所有上述药品的上市许可持有人均应当依据《药品注册管理办法》等有关规定,按照附件要求修订说明书,于2025年6月4日前报省级药品监督管理部门备案。
根据修订要求,炎琥宁注射剂须黑框警告“接受本品治疗的患者有发生严重过敏反应的风险,包括过敏性休克,严重者可导致死亡。6岁及以下儿童禁用本品”。不良反应增加了“皮肤及皮下组织、胃肠系统、全身及给药部位反应、免疫系统、呼吸系统、神经及精神、心血管系统、眼部、血液系统及其他”等十项。修订要求还指出,“本品应单独使用,不宜与其他药品配伍使用。与其他药品序贯使用时应更换输液器。本品有与10%葡萄糖注射液配伍后出现混浊的报告,避免配伍使用。”

国家药监局要求,药品上市许可持有人应当在备案后9个月内对已出厂的药品说明书及标签予以更换或以其他形式将说明书更新信息告知患者,并应在本公告发布后及时将黑框警告内容告知患者和使用单位。对于集中采购中选品种,应确保集采供货药品附以更新的说明书和标签。
米内网数据显示,2023年炎琥宁注射剂在中国三大终端六大市场销售额超过12亿元,同比增长34.38%。2024年年底,炎琥宁注射剂被纳入第三批全国中成药采购联盟集采。根据《医药经济报》报道,注射用炎琥宁是此次集采竞争最为激烈的品种之一,吸引了31家企业申报,共有52个品规参与竞争;同时约定采购量也是最高的一组,预约采购量超过1.07亿支,产品平均降价86%。
公开披露的信息显示,多家上市公司涉及炎琥宁注射剂销售。
集采方面,根据珍宝岛、一品红两家上市公司披露的中标信息,珍宝岛200mg/支的规格的中标价格是0.98元,一品红80mg/1瓶的中标价格为2.20元。
其中,注射用炎琥宁为珍宝岛的第二大单品,2023年和2024年销售持续增长。
根据珍宝岛对于上证所关于2023年年报信息披露监管工作函的回复公告,公司注射用炎琥宁在2023年销售量增加了72%,销售收入为3.21亿元,销售收入增加2.05亿元。2024年,珍宝岛的注射用炎琥宁销售持续增长。根据公司在中标集采公告中披露的数据,珍宝岛的注射用炎琥宁在2024年前三季度销售额达到4.12亿元,在医药工业板块营业收入中占比达到23.50%。
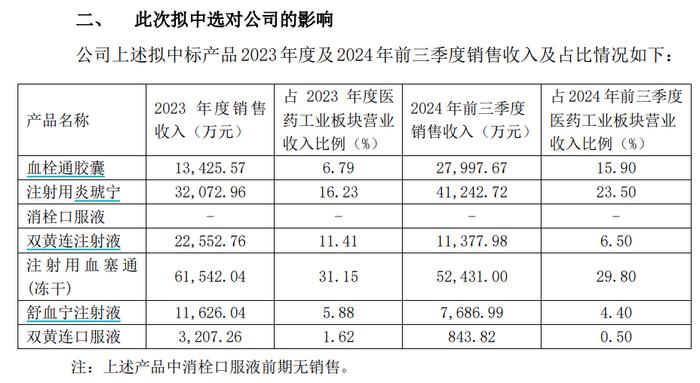
一品红方面披露,注射用炎琥宁2023年度的销售收入为2853万元,占公司2023年度营业收入总额的1.14%。
哈三联在2023年年报中提及,重点产品注射用炎琥宁销量超4000万支。复星医药将注射用炎琥宁列为抗感染核心产品,莱美药业的主要产品中,注射用炎琥宁在列其中。
除了上述几家上市公司,重庆药友制药也是炎琥宁注射剂的销售大户。据米内网数据,重庆药友制药的注射用炎琥宁2023年在中国公立医疗机构终端销售额超过5亿元,增长率22.17%。不过在2024年的集采中,重庆药友制药的40mg品规产品并未中选。
中药注射剂市场不断萎缩
关于“炎琥宁注射剂”的安全,最早可以追溯到16年前。2009年,原国家食品药品监督管理总局就曾通报过炎琥宁的安全性问题,提示儿童患者应当谨慎用药。
事实上,围绕着中药注射剂的安全性争议从未停息,而中药注射剂的市场也在不断萎缩。据摩熵医药数据显示,近年来中药注射剂全国医院全终端市场规模断崖式下跌,从2015年的831.3亿元缩水至2023年的479.8亿元,市场缩水近50%。
在二级市场上,相关企业的销售萎缩甚至滑向退市边缘。
2025年开年,A股5家药企拉响退市警报,其中两家企业与中药注射剂的萎缩密切相关。龙津药业是曾经的中药注射剂龙头企业,大理药业曾经靠醒脑静注射液年入2亿元的企业,市值一度冲破50亿。
市场萎缩的背后,监管层也在对中药注射剂的使用不断提出更加明确和严格的限定。
2017年2月,新版《国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)》出台,对于中药注射剂使用进行了严格的限制,双黄连注射液、丹参注射液、红花注射液等多个品种限二级以上医疗机构使用。
同年10月,中共中央办公厅、国务院办公厅印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,提出对已上市药品注射剂进行再评价,严格控制口服制剂改注射制剂,口服制剂能够满足临床需求的,不批准注射制剂上市。
2019年,新版医保药品目录对中药注射剂提出了更明确、更严格的要求,多个中药注射剂被要求二级以上医疗机构才能使用,同时规定只能用在重症或特定病种上。
2023年,国家药监局组织制定了《中药注册管理专门规定》,其中指出“能选择口服给药的不选择注射给药。”“中药、天然药物注射剂上市后,持有人应当开展药品上市后临床研究,不断充实完善临床有效性、安全性证据,应当持续收集不良反应信息,及时修改完善说明书,对临床使用过程中发现的非预期不良反应及时开展非临床安全性研究。持有人应当加强质量控制。”该规定还提到,“中药说明书【禁忌】、【不良反应】、【注意事项】中任何一项在本规定施行之日起满 3 年后申请药品再注册时仍为‘尚不明确’的,依法不予再注册”。








![[疑问] [疑问]](https://n.sinaimg.cn/commnet/2018new_ningwen_org.png)