半小时观察:欣弗风波揭开谜底 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| http://www.sina.com.cn 2006年08月16日08:32 央视《经济半小时》 | |||||||||
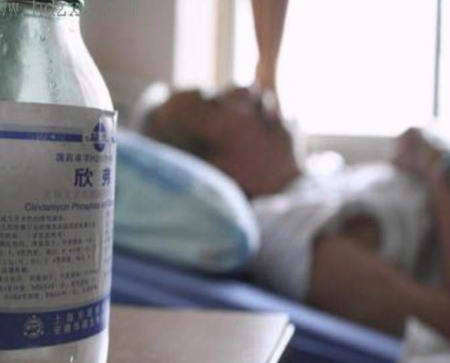 经中国药品生物制品检定所检测表明,安徽华源生物药业有限公司违反规定生产,造成该公司2006年6月至7月生产的克林霉素磷酸酯葡萄糖注射液,无菌检查和热原检查不符合规定。  7月28日,国家药监局的调查组驻安徽华源生物药业有限公司,进行封闭式调查。  安徽省药监局和阜阳市药监局在“欣弗”事件中互相踢起了监管的“皮球” 央视《经济半小时》8月15日播出节目《半小时观察:欣弗风波,揭开谜底》,以下为相关节目内容实录: 最近一阵子,全国各地都被一种叫欣弗的注射液搅得不得安宁,8月2日湖南一位叫陈
为什么本该救人一命的欣弗,会把患者推向绝境?问题药的问题究竟出在哪里?今年,国家食品药品监督管理局正式公布了对欣弗的最后调查结果。 灭菌效果不达标是导致欣弗事件的主要原因 “现已查明安徽华源生物药业有限公司违反规定生产是导致这起不良事件的主要原因,经查该公司2006年6月至7月生产的克林霉素磷酸酯葡萄糖注射液,未按批准的工艺参数灭菌、降低灭菌温度、缩短灭菌时间、增加灭菌柜装载量,影响了灭菌效果,经中国药品生物制品检定所对相关样品进行检测,结果表明,无菌检查和热原检查不符合规定。” 现已查明,生产安徽华源生物药业有限公司自2006年6月份一共生产该产品3701120瓶,售出3186192瓶,除未售出的484700瓶已被封存外,截至8月14日13点,企业已收回1247574瓶,收回途中173007瓶,异地查封403170瓶,这样算下来,尚未收回1362441瓶。 “国家食品药品监管局责成安徽省食品药品监督管理局对安徽华源生物药业有限公司的违法违规行为依法做出处理,并追究相关责任人的责任。” 那么,谁来为此次药品出现质量问题负责? “药品生产企业是药品质量责任的主体,药品生产过程是一个动态过程,药品经过认证不等于进了保险箱,一切都万事大吉,药品组织认证出来了,而是实实在在有药品生产企业出来,药品生产企业都必须严格遵守相关规定,作为药品的主体药品生产主体企业,必须把药品贯彻药品生产的始终,要常抓不懈。” 又该如何杜绝此类事件的发生? “药品生产企业必须建立健全质量保证体系;必须保证每个环节按照标准操作规程执行;必须对原辅料的购入、检验使用等严格管理;必须严格按照法定标准,批准工艺组织生产;必须建立真实的药品生产记录和销售记录;必须保证产品检验合格后审核放行,确保药品生产质量。” 欣弗事件终于真相大白了,但它带来的危机并没有消除,现在仍有136万瓶欣弗下落不明,而且部分流入偏远农村,销售渠道复杂,为查控带来很大困难,也存在着很大隐患。 药监局的反思 7月28日,国家药监局的调查组驻安徽华源生物药业有限公司,进行封闭式调查。 调查组进驻5天后,8月2日,湖北省又有一名患者死亡,此前他也被注射了“欣弗”,同时,国家卫生部统计:青海、广西、浙江、黑龙江、山东等地区,一些患者使用安徽华源生物药业有限公司生产同一批次“欣弗”后,出现胸闷、心悸、寒战、肾区疼痛、过敏性休克、肝肾功能损害等临床症状。 8月3日,卫生部发出紧急通知:全国紧急暂停使用安徽华源生物药业有限公司今年6月份以来生产的所有批次的克林霉素磷酸酯葡萄糖注射液;同时在全国范围内封存尚未使用的此药品。 “欣弗”事件中,一大疑问是,它的质量是否合格?8月4日,安徽华源生物药业首次承认,他们可能存在质量问题。 “现在就是生产工艺上,可能在消毒方面出了问题。” 那么安徽华远生物药业又是怎么消毒的呢? “新的消毒柜在消毒时间上缩短了是吗?” “对,消毒时间上缩短了。” “缩短了多少?” “我们只是缩短了一分钟。” 另外,记者调查中也发现,“欣弗”注射用水的生产设备已经过了有效期,面对药品质量的疑问,8月6日,安徽省药监局发布消息,“欣弗”进行的抽检中,9项检测指标符合国家标准,但最关键的无菌项目是否达标,要等到8月14日才能有结果,此外,“欣弗”事件中,另一大疑问是,造成患者死亡的药物,是怎么出厂的?8月5日,安徽华源生物制药厂门前聚集了来自全国的媒体和群众,面对记者,企业表示。 “把关是质检部门,它化验合格就可以出厂,进入流通。” 但记者来到安徽华源生物制药有限公司质检部门求证时,他们却把自己反锁在大门内,不肯接受采访,那么,“欣弗”的生产,当地的药监部门又是怎么监管的呢? “那么我们就是监督它有没有、符不符合这个标准,有没有严格按照这个标准去执行。” 那么,谁又应该对华源生产出来“欣弗”进行检查呢? “到企业去抽检,这是由市局去抽检。” 那么,阜阳市药监局又是怎么抽检的呢? “省里面给我们的抽查计划一般不叫我们去企业抽查。” 安徽省药监局和阜阳市药监局在“欣弗”事件中互相踢起了监管的“皮球”。 8月10日,国家食品药品监督管理局初步分析认定,安徽华源生物药业有限公司未按批准的生产工艺进行生产,生产记录不完整,这有可能是导致克林霉素磷酸酯葡萄糖注射液(欣弗)集中出现不良事件的原因,而此前,安徽华源生物制药表示,他们的产品没问题。 “从各个地市药检所,有省级的、有地级市的药检所化验出来,我们的产品是合格的。” 8月15日上午10点,国家食品药品监督管理局公布“欣弗”样品的检验结果:无菌检查和热原检查不符合规定。 现在,安徽华源生物制药有限公司已经全面停产,而欣弗事件给企业带来的后果,副总经理徐汉成只说了四个字。 “灭顶之灾。” 相关专题:卫生部通知停用药品欣弗 |
| 新浪首页 > 新闻中心 > 国内新闻 > 卫生部通知停用药品欣弗专题 > 正文 |
| |||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||



