原标题:疫苗安全无小事,看看各国如何严加监管
近日,劣质疫苗事件在票圈掀起轩然大波。大家纷纷对国内疫苗生产、销售、监管等问题提出质疑。
其实,西方国家也曾发生过严重的问题疫苗事件,甚至一度让民众对疫苗的信赖度降至冰点。
但好在一些国家从此类事件中吸取教训,建立起较为完备的疫苗监管机制。
“歪果仁”是如何监管疫苗的呢?
英国:上市前后持续监测
根据英国国民健康保健服务(NHS),一种疫苗从一个想法的诞生到开发成功再到投入使用要花费多年时间。例如,B群脑膜炎球菌疫苗进入市场就花了将近20年的时间。
简单来说,一种疫苗在投入使用前主要经过测试、许可和后期监测三个阶段。

首先,研发机构要在实验室进行测试和开发,测试对象通常是小白鼠。一种疫苗必须在这个阶段通过严格的安全测试,并证明它在动物身上起作用。
之后,疫苗要通过三个阶段的人体临床试验。最初的试验涉及100人左右的成年参与者,他们通常都是志愿者。这一阶段的试验是为了确保疫苗不会在人体身上产生重大安全问题,同时研究人员也要以此找出最有效的剂量。
第二阶段试验涉及几百名参与者,研究人员要检查疫苗是否一致,并观察它是否产生免疫反应,同时开始寻找潜在的副作用。
第三阶段的试验会涉及更广泛的人群,以此收集关于疫苗安全性的数据,得出它的工作原理。这一阶段的研究必须提供证据表明疫苗可以减少病例的数量,能达到预防某种疾病的免疫水平。
在所有的测试都结束后,英国药品和保健产品监管机构(MHRA)或欧洲药品局(EMA)会对所有实验数据进行检查试验和审议,通过审议的则会获得生产许可。
虽然疫苗在生产商获得许可前就进行了严格的测试,但英国对于疫苗的安全性监测是持续的。
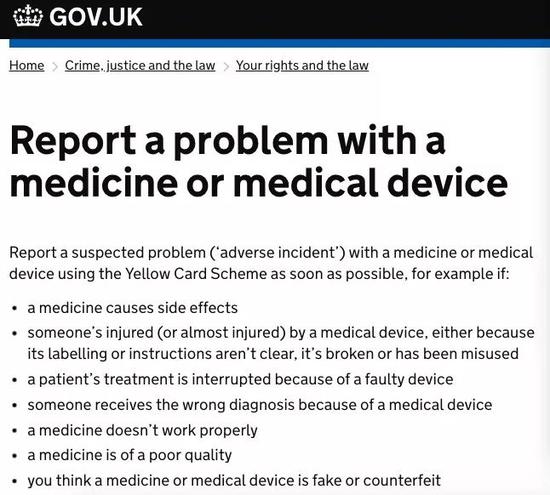
MHRA针对包括疫苗在内的所有获得许可的药物展开了“黄卡计划”。任何人都可以登录黄卡计划官网对所有药物产生的安全隐患或副作用进行报告。
MHRA每周都会对这些数据进行评估,并将报告的副作用与疫苗信息表中详细描述的预期副作用进行比较。如果一个先前未确认的反应出现,或者反应的频率与预期的不一致,那么MHRA将会仔细研究,并视情况发出警告或停用疫苗。
日本:健全的赔偿制度
上世纪六七十年代,日本曾发生多起疫苗副作用事件。
1975年,日本发生两例百日咳DPT疫苗致死事件。该疫苗被停用后再次投入使用时,接种率一度跌到14%,造成百日咳大流行。
在那之后,日本通过开发改良的百日咳疫苗结束了风波。不过,由于日本民众对疫苗副作用的担心,以及日本医疗机构“但求无过”的心态,日本对引进新疫苗一度十分慎重。
直到2009年,厚生劳动省设立了预防接种部,才加速推动了预防接种制度的完善。
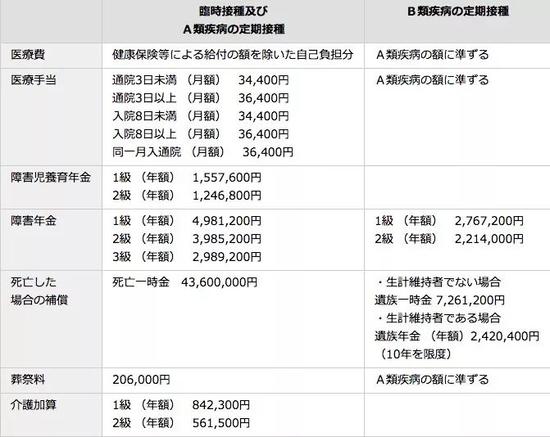
同时,在此期间,日本也逐渐建立起应对问题疫苗及疫苗副作用的应急机制,其中包括建立健全的健康被害赔偿制度。
根据日本厚生劳动省的官网信息,认为自己因为注射疫苗而受到健康损害的公民可以向当地政府申请赔偿,当地政府会将情况反映给厚生劳动省,厚生劳动省会听取疾病障害认定审查会的意见给出最终赔偿方案。
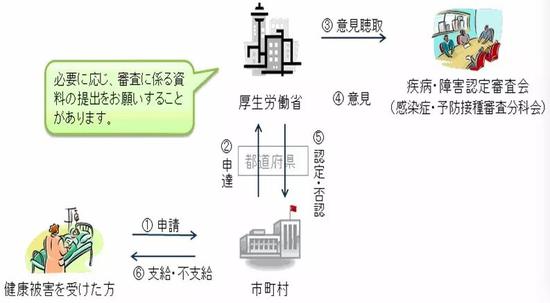
根据厚生劳动省公示的最新资料,一般来说,如果因接种A类疾病(百日咳、麻疹、破伤风、水痘等)疫苗而导致健康损害,受害人若入院3日以内,除了按国民健康保险获得相应补偿外,还应获得医疗赔偿34400日元(约合人民币2101元);受害人若是儿童,最多会获得1557600日元赔偿;受害人若是老年人,最多获得4981200日元的赔偿;如果受害人死亡,应赔偿家属4360万日元。
美国:公开透明的监管渠道
1955年,美国中西部约20万名儿童因接种有问题的脊髓灰质炎疫苗而导致4万名儿童患上脊髓灰质炎,200名儿童患不同程度的瘫痪,10名儿童死亡。
这起事件就是著名的“卡特事件”,美国也从包括该事件在内的一系列问题疫苗事件中汲取教训,建立起长效的监管机制。

在美国,类似于英国的疫苗安全监测机制和不良反应报告系统已相当完善,类似于日本的国家儿童疫苗赔偿伤残赔偿法案(NCVIA)也于上世纪八十年代开始实施。
此外,美国还建立起关于疫苗的信息公开机制。
美国疾控中心官网为父母们提供了详细的疫苗解读,从疫苗测试到生产、投入市场都一目了然。

美国免疫接种咨询委员会(ACIP)也会为父母们提供相关疫苗的各种信息,包括疫苗的安全性和效用如何、其安全性如何被监督和保证等。
1988年,美国健康和人口服务部建立了国家疫苗伤残赔偿项目,该项目会定期出具报告,公开各种疫苗的流通数量和受到诉讼数量的信息。
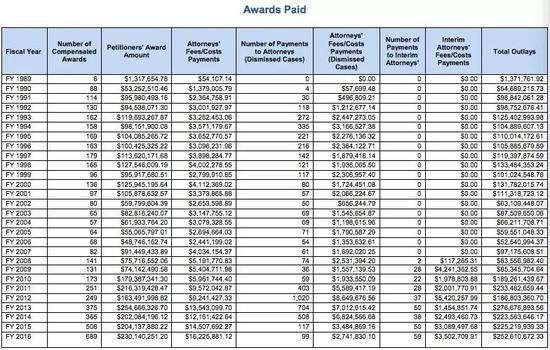
除了政府自主建立透明的信息平台外,媒体行业也在推动信息公开方面起到了重要作用。
2010年,非盈利新闻调查网站ProPublica与《纽约时报》周末副刊共摘普利策调查性报道奖。这篇报道描写新奥尔良市一家医院医护人员在卡特里娜飓风来袭期间的生死抉择。
ProPublica长期以来关注医疗领域,并将传统的调查报道与数据新闻的呈现方式相结合,就多个民众关心的医疗问题进行深入而直观的报道,为读者提供了第一手的医疗信息和内幕。
文/方辰、米勒
相关新闻
官方表态
各地回应
起底药企
媒体评论

更多猛料!欢迎扫描左方二维码关注新浪新闻官方微信(xinlang-xinwen)
推荐新闻
- 【 新闻 】 这行业规模可达万亿 将带动3000万人就...
- 【 军事 】 出鞘:如何看土耳其山寨中国技术搞两...
- 【 财经 】 国航乘客亲述急降12分钟:至今没有道歉
- 【 体育 】 托雷斯正式亮相J联赛 举9号战袍露笑容
- 【 娱乐 】 周立波案“某某”受访否认是贪二代
- 【 科技 】 李克强就疫苗事件作批示:必须明白交代
- 【 教育 】 高校通知书 当心打助学旗号的电信诈骗
违法和不良信息举报电话:010-62675637
举报邮箱:jubao@vip.sina.com
Copyright © 1996-2018 SINA Corporation
All Rights Reserved 新浪公司 版权所有






















